Mamitis bovina: patogenia y manifestaciones clínicas
En nuestra primera publicación sobre mamitis bovina hablamos acerca de la definición, etiología y epidemiología de esta enfermedad, que como bien sabéis es bastante común en la especie bovina. Continuando con la serie de entradas sobre esta patología hoy os trataremos tanto la patogenia como las manifestaciones clínicas que podemos encontrarnos.

El correcto ordeño y manejo es muy importante a la hora de prevenir la mamitis (foto de Michael Coghlan)
PATOGENIA
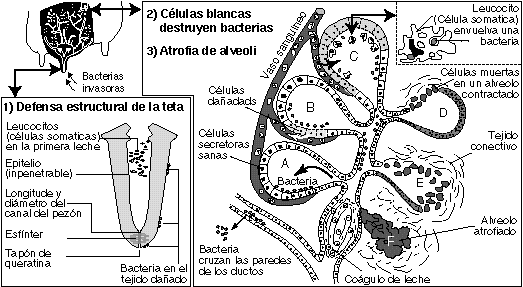
Salvo en la tuberculosis, en la cual el método de diseminación puede ser hematógena, la infección de la glándula mamaria se produce siempre siguiendo la vía del conducto del pezón, y a simple vista el desarrollo de la inflamación después de la infección se considera un fenómeno natural. Sin embargo, el desarrollo de mastitis es más complejo y se puede explicar en tres etapas: invasión, infección e inflamación del área dañada y destrucción del tejido alveolar.
Invasión
En prácticamente todos los casos, las bacterias causantes de la mastitis penetran a la glándula mamaria a través del canal del pezón, que se convierte en la primera y más importante barrera de defensa de la glándula mamaria. De ahí la gran importancia de reducir la carga microbiana de la piel del pezón y preservar la funcionalidad del canal y del esfínter, antes que las bacterias penetren y colonicen el parénquima, porque en este último caso, ocurre la respuesta inflamatoria y con ella el daño al epitelio secretor y a la calidad de la leche. Considerando lo pequeño de la longitud del canal (8-15 mm), la estructura microscópica y bioquímica del canal son muy efectivas en evitar la penetración bacteriana, incluyendo el estado funcional del esfínter. Si bien en la estructura de la queratina se han caracterizado proteínas catiónicas y algunos ácidos grasos de cadena larga con actividad bactericida, ahora se sabe que no son activas “in vivo”. Ciertas características físicas del canal del pezón parecen jugar un papel más importante en el mecanismo de defensa del canal, entre ellas el largo del canal, el diámetro máximo que alcanza al momento del flujo máximo de leche (entre los 2-3 minutos de ordeño) y la masa descamable de queratina. Se ha demostrado una mayor susceptibilidad a las nuevas infecciones, tanto durante la lactancia como en los primeros días después del secado, en aquellas vacas con flujos máximos de leche muy altos. También la presencia de una masa íntegra de queratina es de importancia para impedir la prevención bacteriana, ya que las células de la capa superficial del epitelio queratinizado del canal son capaces de adsorber a las bacterias en una “película” de lípidos extracelulares. Esta película proporciona también una débil adhesión intercelular entre las células queratinizadas viejas ya descamadas, lo que no impide su expulsión por el flujo de leche durante el ordeño. Son entonces la adsorción de las bacterias a la queratina, combinado con su descamación regular fisiológica y su remoción por el flujo de leche, los mecanismos responsables de su capacidad de defensa.
Infección
Es la etapa en la que los gérmenes se multiplican rápidamente e invaden el tejido mamario; se establece una población microbiana que se disemina por toda la glándula, dependiendo de la patogenicidad del microorganismo. El tipo de bacteria determina su capacidad de multiplicarse en la leche y adherirse al epitelio mamario. La virulencia de especies bacterianas individuales al parecer se debe, por lo menos en parte, a esta capacidad de adherencia. La infección se produce más fácilmente en el período de secado, debido a la ausencia de flujo. Se ha aceptado en términos generales este concepto, pero un análisis cuidadoso sugiere que la susceptibilidad es alta en el período de secado, aunque mucho menor en el cuarterón glandular que ha permanecido seco durante algún tiempo.
Inflamación del área dañada
Una vez que las bacterias (o sus toxinas) superan la línea de defensa del canal del pezón y alcanzan los tejidos altos, comienza a operar la segunda línea de defensa, que incluye a factores humorales inespecíficos presentes en la leche o secreción de la ubre seca (lactoferrina, inmuno-lacto-peroxidasa, lizosima, fracciones del complemento y otros compuestos químicos) y los mecanismos de defensa inmunológicos o específicos, ya sea de tipo humoral (inmunoglobulinas y otros factores solubles) o de base celular, incluyendo el sistema fagocítico (macrófagos (MA) y PMN) y el sistema linfocitario (linfocitos T, B y sin clasificar). Polimorfonucleares, macrófagos, linfocitos y escasas células epiteliales constituyen las llamadas células somáticas.
En la glándula mamaria, como en cualquier otro tejido, la respuesta inflamatoria involucra tres etapas, jugando un rol central el sistema microcirculatorio:
- ETAPA 1: El proceso inflamatorio comienza con una reacción del endotelio de los capilares cercanos a las células alveolares atacadas por las bacterias. Durante esta fase aguda, se incrementa tanto el flujo sanguíneo en el lecho capilar como la permeabilidad del endotelio, ya que las células endoteliales se contraen, dejando espacios entre ellas que permiten el paso al intersticio de proteínas sanguíneas, iones y agua, causando edema. Los PMN sanguíneos comienzan a adherirse al endotelio.
- ETAPA 2: En esta fase subaguda, los macrófagos y polimorfonucleares migran desde la sangre y del intersticio circundante a los alvéolos infectados y a la leche. Los macrófagos funcionan como las células de la “alarma temprana”, reconociendo a toda substancia extraña al cuerpo. La función de los polimorfonucleares es la de fagocitar y destruir a los microorganismos invasores y a cualquier otro tipo de proteína foránea y remover los deshechos producidos en el foco de infección.
Debido a la alteración de la barrera endotelio capilar- epitelio mamario hay un paso anormal de componentes del plasma sanguíneo a la leche (el plasma sanguíneo contiene proteasas y lipasas que aceleran la descomposición de la grasa y la proteína de la leche y plasmita, una enzima proteolítica que puede causar daño extenso a la caseína). Al mismo tiempo que aumenta el número de células somáticas en la leche, comienzan también los cambios en la composición de la leche. La cantidad de lactosa en leches con mamitis disminuye y, para mantener el balance osmótico de la leche se cambia el perfil mineral de la leche. También se afectan las concentraciones de algunas vitaminas hidrosolubles de la leche (esto afecta a la capacidadde fermentación).
- ETAPA 3: El final del proceso inflamatorio (fase crónica proliferativa) implica la disminución o el cese de la actividad sintética y secretoria, la degeneración y lisis de las células alveolares y su reemplazo por tejido conectivo afuncional, con la consiguiente pérdida en producción.
MANIFESTACIONES CLÍNICAS
Según la resistencia del tejido mamario y la virulencia de las bacterias invasoras, pueden observarse todos los grados de intensidad en los signos, desde comienzo gradual por fibrosis, pasando por inflamación aguda sin reacción sistémica, hasta toxemia grave con signos sistémicos manifiestos.
Muchas de las especies de bacterias que provocan mamitis pueden producir formas sobreagudas, agudas y crónicas de la enfermedad, generalmente es imposible establecer una diferenciación clínica de los tipos bacteriológicos de mamitis.
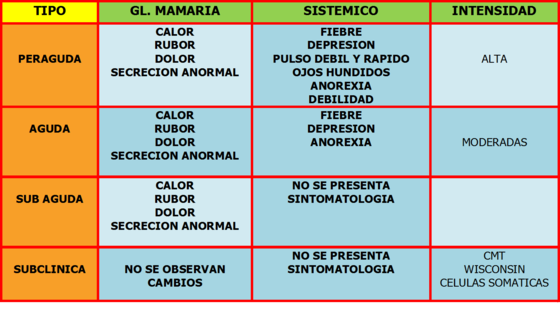
Los síntomas clínicos de la mastitis incluyen anormalidades de la secreción, tamaño, consistencia y temperatura de la glándula mamaria, y con frecuencia reacción sistémica. Las formas clínicas de mastitis suelen clasificarse según su gravedad:
1. Mamitis clínicas.
- Sobreaguda: inflamación intensa de uno de los cuarterones de la glándula mamaria con reacción sistémica intensa.
- Aguda: inflamación grave sin reacción sistémica.
- Subaguda: inflamación leve con anormalidades persistentes de la leche.
- Crónicas: con ataques recurrentes de inflamación con poco cambio en la leche.
2. Mamitis subclínicas
Se dice que la mamitis es subclínica cuando hay evidencia de inflamación; por ejemplo, recuento elevado de células somáticas en la leche sin anormalidad visibles de leche o ubre.
Anomalías de la leche
El examen de la leche requiere el empleo de una copa para el análisis preferentemente con fondo negro brillante que permita la identificación de los cambios de color o la presencia de coágulos, copos o pus. La leche se vierte sobre la copa en pequeñas cantidades comparando la procedente de los diferentes cuarterones.
Puede estar teñida de sangre o con aspecto acuoso; esto último indica mastitis crónica cuando el cuarterón del que procede está en fase de lactación. Cuando la leche tiene aspecto acuoso durante los primeros chorros de ordeño, no se le da importancia, pero si persiste después de varias extracciones debe considerarse anormal.
Los coágulos de leche o copos suelen acompañarse de cambios de color y son siempre significativos, ya que suelen indicar un grado intenso de inflamación, incluso cuando son pequeños y sólo se observan en los primeros chorros. Los coágulos de sangre normalmente carecen de importancia, así como los pequeños tapones céreos que se observan a menudo en la leche durante los primeros días del puerperio, sobre todo en primíparas. La presencia de copos al final del ordeño suele indicar tuberculosis mamaria en bovinos. Durante el período seco en vacas normales, la leche cambia desde leche normal a un líquido acuoso claro, después de una secreción y consistencia de la miel y, por último, a calostro en los pocos días que preceden al parto. Pueden registrarse variaciones entre cada uno de los cuarterones de la glándula en una vaca, que si son notables justifican la sospecha de infección.
Anomalías de la ubre
Cabe comprobar por la vista y el tacto las anormalidades de tamaño y consistencia de los cuarterones. Procede observar la glándula desde atrás en sus dos cuarterones posteriores en busca de asimetría. Elevando dichos cuarterones pueden apreciarse los dos anteriores. La decisión de definir qué cuarterón de un par es anormal puede depender de la palpación, que debe efectuarse sobre cuarterones adyacentes simultáneamente. Si bien, en la mayor parte de las formas de mastitis las anomalías observadas se hallan principalmente en la región de la cisterna de la leche, debe palparse el cuarterón en su totalidad. Sin embargo, es importante también palpar los pezones y ganglios linfáticos supramamarios, y buscar en los primeros la presencia de úlceras, sobre todo alrededor del esfínter.
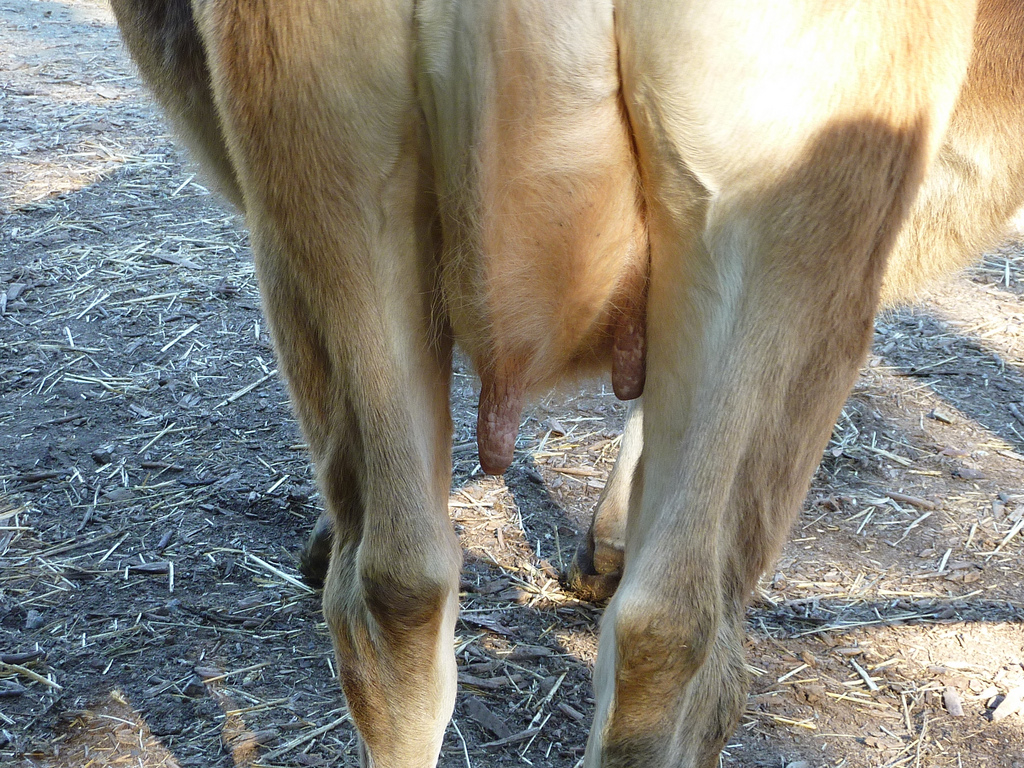
Debemos hacer una exploración exhaustiva a la hora de detectar las anomalías en la ubre (foto de Eugene Kim)
La palpación e inspección de la ubre tiene por finalidad descubrir fibrosis, edema inflamatorio y atrofia del tejido mamario; la fibrosis puede presentarse en varias formas. Puede haber aumento difuso del tejido conectivo, lo que da al cuarterón una sensación de firmeza superior a la del opuesto, y casi siempre una superficie más nodular por palpación ligera. Es también posible la aparición de áreas locales de fibrosis de un cuarterón, que puede variar el tamaño desde lesiones como guisantes hasta masas tan grandes como un puño. La inflamación aguda es siempre difusa y se acompaña de calor, dolor y anormalidad manifiesta de la secreción. En casos graves pueden comprobarse áreas de gangrena, o aparición de abscesos en el tejido glandular. La etapa terminal de la mastitis crónica es la atrofia de la glándula. Por examen casual puede clasificarse un cuarterón atrofiado como normal, a causa de su pequeño tamaño, mientras que el cuarterón normal se juzga como hipertrofiado. La palpación cuidadosa revela, con frecuencia, la escasa incapacidad funcional del tejido mamario en el cuarterón atrofiado.
Reacción sistémica
Según el tipo y gravedad de la infección pueden comprobarse o no signos sistémicos como toxemia, fiebre, depresión general y anorexia.
En próximos artículos hablaremos del diagnóstico, tratamiento y de los posibles hallazgos en necropsia de animales que han fallecido, por ejemplo, debido a toxemia aguda.
Referencias
José Manuel López Rodríguez
Latest posts by José Manuel López Rodríguez (see all)
- Mamitis bovina: diagnóstico y tratamientos - 14 de julio de 2014
- Mamitis bovina: patogenia y manifestaciones clínicas - 11 de julio de 2014
- Mamitis bovina: definición, etiología y epidemiología de la enfermedad - 28 de mayo de 2014